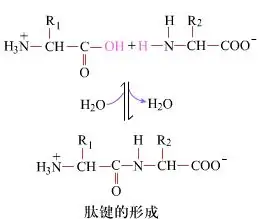
En surface, la formation de liaisons peptidiques, donnant des dipeptides, est un processus chimique simple.Cela signifie que les deux composants acides aminés sont liés par une liaison peptidique, une liaison amide, tout en étant déshydratés.
La formation de liaisons peptidiques est l’activation d’un acide aminé dans des conditions de réaction douces.(A) fragment carboxyle, deuxième acide aminé (B) Le fragment carboxyle activé nucléophile forme ensuite le dipeptide (AB)."Si le composant carboxyle (A) n'est pas protégé, la formation de la liaison peptidique ne peut pas être contrôlée."Les sous-produits tels que les peptides linéaires et cycliques peuvent être mélangés aux composés cibles AB.Par conséquent, tous les groupes fonctionnels non impliqués dans la formation de liaisons peptidiques doivent être protégés de manière temporairement réversible lors de la synthèse peptidique.
Ainsi, la synthèse peptidique – la formation de chaque liaison peptidique – implique trois étapes d’agrégation.
La première étape consiste à préparer certains acides aminés qui ont besoin d’être protégés, et la structure zwitterionique des acides aminés n’existe plus.
La deuxième étape est une réaction en deux étapes pour former des liaisons peptidiques, dans laquelle le groupe carboxyle de l'acide aminé N-protégé est d'abord activé en intermédiaire actif, puis la liaison peptidique est formée.Cette réaction couplée peut se produire soit sous la forme d’une réaction en une étape, soit sous la forme de deux réactions séquentielles.
La troisième étape est le retrait sélectif ou complet de la base de protection.Bien que toute élimination ne puisse avoir lieu qu’une fois que toutes les chaînes peptidiques ont été assemblées, l’élimination sélective des groupes protecteurs est également nécessaire afin de poursuivre la synthèse peptidique.
Parce que 10 acides aminés (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec et Cys) contiennent des groupes fonctionnels de chaîne latérale, qui nécessitent une protection sélective, ce qui rend la synthèse peptidique plus compliquée.Les bases de protection temporaires et semi-permanentes doivent être distinguées en raison des différentes exigences de sélectivité.Les groupes de protection temporaire sont utilisés à l’étape suivante pour refléter la protection temporaire des groupes fonctionnels acides aminés ou carboxyles.Les groupes protecteurs semi-permanents sont éliminés sans interférer avec les liaisons peptidiques ou les chaînes latérales d'acides aminés déjà formées, parfois pendant la synthèse.
"Idéalement, l'activation du composant carboxyle et la formation ultérieure de liaisons peptidiques (réactions de couplage) devraient être rapides, sans formation racémique ou sous-produit, et des réactifs molaires devraient être appliqués pour obtenir des rendements élevés."Malheureusement, aucune des méthodes de couplage chimique ne satisfait à ces exigences et rares sont celles qui conviennent à une synthèse pratique.
Lors de la synthèse peptidique, les groupes fonctionnels impliqués dans diverses réactions sont généralement liés au centre manuel, la glycine étant la seule exception, et il existe un risque potentiel de rotation.
La dernière étape du cycle de synthèse peptidique est l’élimination de tous les groupes protecteurs.L'élimination sélective des groupes protecteurs est importante pour l'extension de la chaîne peptidique en plus de l'exigence d'une élimination complète de la protection dans la synthèse des dipeptides.Les stratégies synthétiques doivent être soigneusement planifiées.En fonction du choix stratégique, N peut éliminer sélectivement les groupes protecteurs α-amino ou carboxyle.Le terme « stratégie » fait référence à la séquence de réactions de condensation d’acides aminés individuels.En général, il existe une différence entre la synthèse progressive et la condensation de fragments.La synthèse peptidique (également appelée « synthèse conventionnelle ») s’effectue en solution.Dans la plupart des cas, l’allongement progressif de la chaîne peptidique ne peut être synthétisé qu’en utilisant la chaîne peptidique pour synthétiser des fragments plus courts.Pour synthétiser des peptides plus longs, les molécules cibles doivent être segmentées en fragments appropriés et déterminés qu'elles peuvent minimiser le degré de différenciation à l'extrémité C-terminale.Une fois les fragments individuels progressivement assemblés, le composé cible sera réuni.La stratégie de synthèse peptidique comprend la sélection du fragment protecteur le meilleur et le plus approprié, et la stratégie de synthèse peptidique comprend la sélection de la combinaison la plus appropriée de bases protectrices et la meilleure méthode de conjugaison des fragments.
Heure de publication : 19 juillet 2023