Technologie de synthèse peptidique
La recherche et le développement de médicaments peptidiques connaissent une croissance rapide en médecine.Cependant, le développement de médicaments peptidiques est limité par leurs propres caractéristiques.Par exemple, en raison de la sensibilité particulière à l'hydrolyse enzymatique, la stabilité est réduite et la variabilité de la conformation stérique entraîne une faible spécificité de ciblage, une faible hydrophobicité et l'absence d'un système de transport spécifique.Afin de vaincre ces peptides, de nombreuses solutions ont été proposées et l'application réussie d'un type de peptide en fait partie.
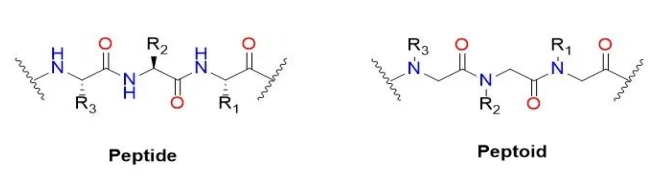
Sorte de peptide (nom anglais : Peptoid) ou Poly – N – à la place de la glycine (nom anglais : Poly real – N – substituedglycine), c'est un composé quasi peptidique de peptide dans la chaîne principale.La chaîne latérale du carbone alpha transfère l’azote de la chaîne principale au lieu de la chaîne latérale.Dans le polypeptide original, le groupe R de la chaîne latérale des acides aminés représente 20 acides aminés différents, mais le groupe R a plus d'options dans le peptoïde.Dans le peptide, le peptide sur la chaîne principale des acides aminés dans l'azote alpha-carboné au lieu du transfert de la chaîne latérale vers la chaîne principale.Il convient de mentionner que les peptides en général ne produisent pas les mêmes structures ordonnées de haut niveau que les structures secondaires des peptides et des protéines en raison du manque d'hydrogène sur l'azote du squelette.L’objectif initial du peptide est de développer un peptide stable et protéase de médicaments à petites molécules.
Analyse des techniques de synthèse peptidique
La méthode de synthèse peptidique a été introduite
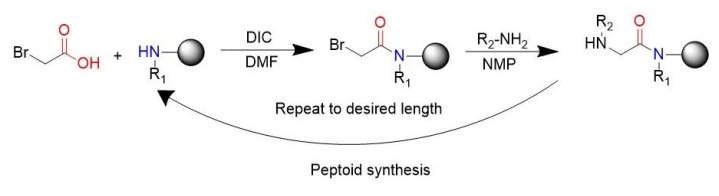
La méthode de synthèse peptidique généralement populaire est la méthode de synthèse subsingle inventée par RonZuckermann, dont chacune est divisée en deux étapes : l'acylation et le déplacement.Lors de l'acylation, la première étape consiste à activer l'acide haloacétique pour qu'il réagisse avec les amines restant à la fin de l'étape précédente, le plus souvent la diimine carbonisée diisopropylique.L'acide bromoacétique a été activé par le diisopropylcarbodiimide."Dans les réactions de substitution (réactions de substitution nucléophiles bimoléculaires), une amine, généralement primaire, attaque l'halogène alternatif pour former une glycine N-substituée."La voie de synthèse sous-unitaire utilise des amines primaires facilement disponibles pour générer des peptides, permettant ainsi la synthèse chimique des peptides.
Une extension solide dans la synthèse de peptides de classe possède une riche expérience et peut vous fournir une variété de types de services de synthèse de peptides.
Analyse des techniques de synthèse peptidique
L'avantage d'un tel peptide
Plus stable : les peptoïdes sont plus stables in vivo que les peptides.
Plus de sélectivité : les peptoïdes conviennent bien aux études combinées de découverte de médicaments, car une grande variété de différents éléments constitutifs polypeptidiques peuvent être obtenus par modification du groupe amino du squelette.
Plus efficace : l'abondance des structures peptoïdes peut faire du peptoïde un bon choix pour la méthodologie d'analyse permettant de trouver rapidement des structures spécifiques qui se lient aux protéines.
Plus de potentiel de marché : les caractéristiques du type de peptide lui permettent de devenir une sorte de développement de médicaments doté d'un grand potentiel.
Heure de publication : 07 décembre 2023