Arrière-plan
Melanotan I, également connu sous le nom d'Afamélanotide, est un polypeptide linéaire composé de 13 acides aminés appelé à jouer un rôle de plus en plus important dans la recherche pharmaceutique. Les principaux noms anglais de Melanotan I sont Melanotan-1 et Afamelanotide. En tant qu'analogue synthétique de l'hormone α-MSH stimulant les mélanocytes), Melanotan I peut être utilisé pour traiter les troubles de la photosensibilité causés par la protoporphyrie érythropoïétique. Actuellement, la plupart des produits Melanotan I sont étiquetés uniquement pour la recherche et ne sont pas encore destinés à une application humaine. Dans la synthèse traditionnelle en phase solide, le choix de la résine a un impact significatif sur l'efficacité du couplage et la pureté finale du produit.
Informations de base
Nom chinois : Mélanotan 1
Nom anglais : Melanotan-1
Numéro d'entreprise : GT-A006
N° CAS : 75921-69-6
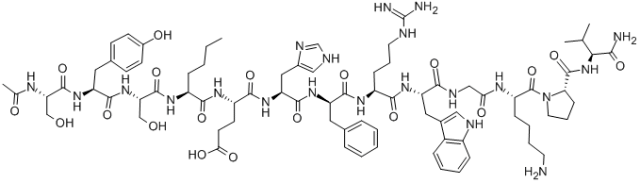
Séquence : SYS{Ne}EH{D-Phe}RWGKPV-NH2
Formule moléculaire : C78H111N21O19
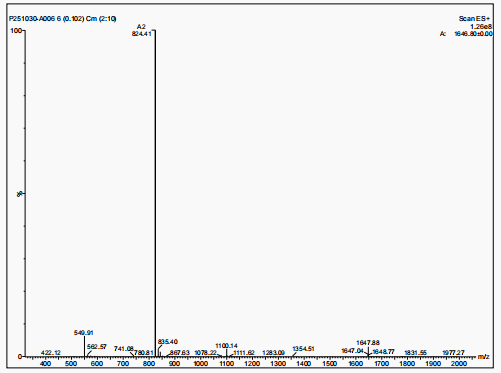
Poids moléculaire : 1646,88
Méthode de préparation
JE. Préparation de la résine Fmoc-Val-Amino
Étape 1 :Pesez 11,11 g (5 mmol) de résine Ramage Amide AM avec un degré de substitution de 0,45 mmol/g et ajoutez-le dans un réacteur en phase solide. Ajouter du DCM pour faire gonfler la résine pendant 30 minutes, puis égoutter. Laver trois fois avec du DMF. Ajouter une solution de DMF contenant 20% de pipéridine (v/v) et réagir pendant 5 minutes. Ajouter une autre solution de pipéridine DMF à 20 % et réagir pendant 10 minutes, avec un lavage au DMF entre les deux. Une fois la réaction terminée, égoutter et laver trois fois avec du DMF.
Étape 2 :Dissoudre 5,09 g de Fmoc-Val-OH, 2,02 g de HOBT (1-hydroxybenzotriazole) et 2,32 ml de DIC (N,N'-diisopropylcarbodiimide) dans du DMF à 0°C. Après dissolution complète, ajouter le mélange dans la colonne de réaction et réagir à température ambiante pendant 1 heure. Surveillez la progression de la réaction à l’aide du test à la ninhydrine, en vous assurant d’un résultat négatif. Une fois la réaction terminée, laver trois fois avec du DMF pour obtenir la résine Fmoc-Val-amino.
II. Préparation du peptide de résine entièrement protégé de Melanotan I.
Étape 1 :Ajouter 20 % de pipéridine dans une solution de DMF (rapport volumique) à la Fmoc-Val-aminorésine ci-dessus. Réagir pendant 5 minutes, puis ajouter une autre portion de pipéridine à 20 % dans une solution de DMF et réagir pendant 10 minutes. Laver une fois avec du DMF pendant l'intervalle. Une fois la réaction terminée, sécher sous vide et laver trois fois avec du DMF.
Étape 2 :Dissoudre 5,06 g de Fmoc-Pro-OH, 2,02 g de HOBT (1-hydroxybenzotriazole) et 2,32 ml de DIC (N,N'-diisopropylcarbodiimide) dans du DMF à 0°C. Après dissolution complète, ajouter le mélange dans la colonne de réaction et réagir à température ambiante pendant 1 heure. Surveiller l'évolution de la réaction à l'aide du test à la ninhydrine (test de Kaiser) jusqu'à l'obtention de résultats négatifs. Une fois terminé, laver trois fois avec du DMF pour obtenir de la Fmoc-Pro-Val-aminoresin.
Étape 3 :En suivant la méthode décrite à l’étape 2, couplez séquentiellement chaque acide aminé selon la séquence de Melanotan I. Après l’achèvement de la réaction de couplage Ac-Ser(tBu)-OH, lavez trois fois avec du DMF, trois fois avec du DCM (dichlorométhane) et trois fois avec du méthanol. Sécher sous vide pour obtenir 23,89 g de peptide lié à la résine Melanotan I entièrement protégé.
III. Préparation du peptide brut Melanotan I
23,89 g de peptide lié à la résine Melanotan I entièrement protégé ont été placés dans un flacon à fond rond. À 0°C, 250 ml d'un cocktail de clivage pré-préparé (composé de TFA : thioanisole : phénol : triisopropylsilane : eau = 82,5 : 7,5 : 5 : 3 : 2 en volume) ont été ajoutés lentement sous agitation. Le mélange a été mis à réagir à basse température pendant 0,5 heure, suivi d'une réaction à température ambiante pendant 2 heures. La solution de clivage a ensuite été filtrée sous vide. Cette solution a été ajoutée lentement à 2 L d'éther diéthylique anhydre glacé sous agitation. Le peptide brut a été isolé par filtration, lavé trois fois avec de l'éther diéthylique glacé, et 8,55 g de peptide brut Melanotan I ont été obtenus.
IV. Préparation du peptide purifié Melanotan I
Étape 1 :Dissoudre le peptide Melanotan I brut dans 100 ml d’eau purifiée et filtrer sur membrane de 0,45 µm pour obtenir une solution de peptide brut.
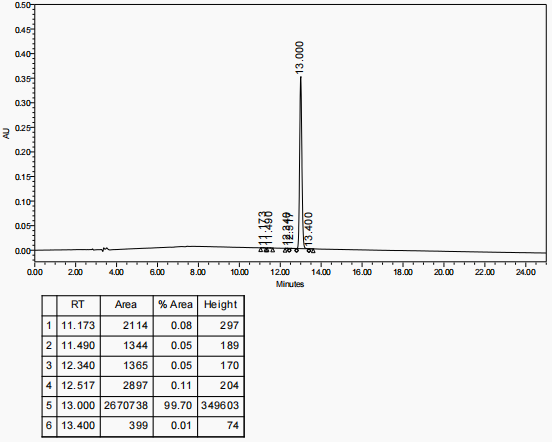
Étape 2 :Purifier le peptide Melanotan I brut par chromatographie liquide haute performance (HPLC). Utilisez une colonne de compression axiale dynamique DAC-HB50 avec la phase mobile A (solution aqueuse d’acide trifluoroacétique à 0,05 %) et la phase mobile B (acide trifluoroacétique à 0,05 % dans l’acétonitrile). Effectuer une élution par gradient pour la séparation et la purification. Détectez l’échantillon à l’aide d’un détecteur UV et collectez la solution peptidique correspondant au pic cible en fractions.
Étape 3 :Après purification HPLC, obtenir 180 ml de solution de trifluoroacétate Melanotan I d'une pureté supérieure à 99%. Concentrer la solution à 50 ml par évaporation rotative.
Étape 4 :Équilibrer la colonne de chromatographie avec de l'eau déminéralisée et charger 50 ml de la solution purifiée de trifluoroacétate Melanotan I (pureté > 99 %). Éluer pendant 50 minutes dans un système de solution aqueuse à 2 % d’acide acétique. Concentrer le produit cible collecté à 80 ml par évaporation rotative. Effectuer une pré-lyophilisation et une lyophilisation pour obtenir finalement 5,33 g de peptide purifié Melanotan I, avec un rendement de 32,33 %.
Heure de publication : 2026-01-05
