Que sont les acides aminés?
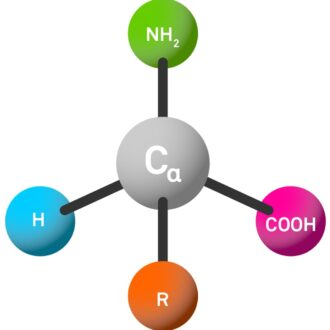
Les acides aminés les plus courants dans la nature sont appelés acides α-aminés. Ces molécules ont quatre substituants différents attachés à l'atome de carbone central (appelé atome α-C):
Amino (NH₂, code à trois lettres abrégé en "H-").
Groupe d'acide carboxylique (COOH, abrégé en "-oh" dans le code à trois lettres).
Chaînes latérales(R, qui sont très variables et déterminent les propriétés des acides aminés ainsi que le peptide final).
Atome d'hydrogène (H).
La connexion des atomes α-C avec ces quatre groupes différents lui donne des propriétés chimiques uniques, qui jouent un rôle clé dans la détermination du comportement et des propriétés des acides aminés et des peptides.
Activité biologique des acides aminés
Les acides aminés peuvent présenter des activités biologiques telles que:
Le tryptophane (TRP) et l'acide glutamique (GLU) jouent un rôle clé dans les processus métaboliques.
Le groupe R (ou la chaîne latérale) détermine les propriétés uniques des acides aminés. Ces groupes peuvent:
En termes simples:Un atome d'hydrogène comme la glycine (Gly).
D'autres acides sont inclus: comme l'acide aspartique (ASP) et l'acide glutamique (GLU).
Transporter des groupes de base:arginine (arg), lysine (lys) ou histidine (sien).
Contient des groupes polaires: comme la sérine (SER) ou la thréonine (THR).
Hydrocarbures non polaires:alanine (ALA), phénylalanine (Phe) ou valine (Val).
Contenu en soufre:comme le montre la cystéine (Cys) et la méthionine (MET).
Le rôle des acides amino L et des acides Amino D
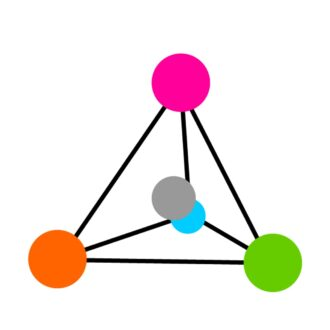
Les quatre substituants de l'atome α-C sont disposés aux coins du tétraèdre, avec l'atome α-C au centre (voir figure 3). Cet arrangement permet aux deux formes de molécules d'acides aminés d'exister sous forme de miroir, similaires aux mains gauche et droite. Ces formes de miroir sont appelées «stéréoisomères» ou «énantiomères».
Importance biologique des énantiomères
Bien que les énantiomères aient des propriétés chimiques et physiques presque identiques, leurs effets biologiques peuvent différer considérablement. La forme moléculaire est essentielle à son interaction avec les cibles biologiques. Un éantiomère peut se lier efficacement à la cible, un autre peut ne pas, ou dans certains cas, avoir un effet négatif. En solution, l'énantiomère tourne le plan de lumière polarisé dans la direction opposée.
Heure du poste: 2025-09-05
