Les peptides sont une classe de composés formés par la connexion de plusieurs acides aminés à travers des liaisons peptidiques. Ils sont omniprésents dans les organismes vivants. Jusqu'à présent, des dizaines de milliers de peptides ont été trouvés dans les organismes vivants. Les peptides jouent un rôle important dans la régulation des activités fonctionnelles de divers systèmes, organes, tissus et cellules et dans les activités de vie, et sont souvent utilisés dans l'analyse fonctionnelle, la recherche sur les anticorps, le développement de médicaments et d'autres domaines. Avec le développement de la technologie de la biotechnologie et de la synthèse des peptides, de plus en plus de médicaments peptidiques ont été développés et appliqués en clinique.
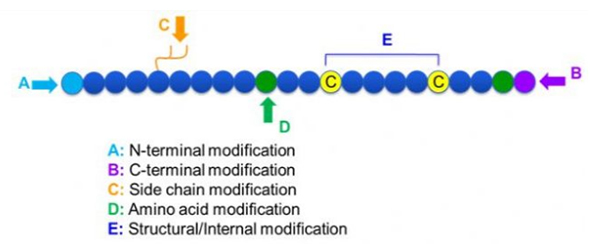
Il existe une grande variété de modifications des peptides, qui peuvent être simplement divisées en post-modification et modification du processus (en utilisant la modification dérivée des acides aminés), et la modification du N-terminal, la modification C-terminale, la modification de la chaîne latérale, la modification des acides aminés, la modification du squelette, etc., selon le site de modification (figure 1). En tant que moyen important de modifier la structure principale de la chaîne ou des groupes de chaîne latérale de chaînes peptidiques, la modification des peptides peut modifier efficacement les propriétés physiques et chimiques des composés peptidiques, augmenter la solubilité de l'eau, prolonger le temps d'action in vivo, modifier leur distribution biologique, éliminer l'immunogénicité, réduire les effets secondaires toxiques, etc.
1. Cyclisation
Les peptides cycliques ont de nombreuses applications dans la biomédecine, et de nombreux peptides naturels avec une activité biologique sont des peptides cycliques. Parce que les peptides cycliques ont tendance à être plus rigides que les peptides linéaires, ils sont extrêmement résistants au système digestif, peuvent survivre dans le tube digestif et présentent une affinité plus forte pour les récepteurs cibles. La cyclisation est le moyen le plus direct de synthétiser les peptides cycliques, en particulier pour les peptides avec un grand squelette structurel. Selon le mode de cyclisation, il peut être divisé en type de chaîne de chaîne latérale, type de chaîne latérale terminale, type de terminal - terminal (type de bout).
(1) Sidechain-to-sidechain
Le type le plus courant de cyclisation de la chaîne latérale à la chaîne latérale est le pontage disulfure entre les résidus de cystéine. Cette cyclisation est introduite par une paire de résidus de cystéine déprotégées puis oxydés pour former des liaisons disulfure. La synthèse polycyclique peut être obtenue par élimination sélective des groupes de protection des sulfhydryles. La cyclisation peut être effectuée soit dans un solvant post-dissociation, soit sur une résine de pré-dissociation. La cyclisation sur les résines peut être moins efficace que la cyclisation du solvant car les peptides sur les résines ne forment pas facilement des conformations cyclifiées. Un autre type de cyclisation de la chaîne latérale de chaîne latérale est la formation d'une structure amide entre un acide aspartique ou un résidu d'acide glutamique et l'acide aminé de base, ce qui nécessite que le groupe de protection de la chaîne latérale doit être enlevé sélectivement du polypeptide sur la résine ou après la dissociation. Le troisième type de cyclisation de la chaîne latérale latérale est la formation d'éthers diphényle par la tyrosine ou la p-hydroxyphénylglycine. Ce type de cyclisation dans les produits naturels ne se trouve que dans les produits microbiens, et les produits de cyclisation ont souvent une valeur médicinale potentielle. La préparation de ces composés nécessite des conditions de réaction uniques, de sorte qu'elles ne sont pas souvent utilisées dans la synthèse de peptides conventionnels.

(2) Terminal à sidechain
La cyclisation de la chaîne du côté terminal implique généralement le C-terminal avec le groupe amino de la chaîne latérale de la lysine ou de l'ornithine, ou le N-terminal avec l'acide aspartique ou la chaîne latérale d'acide glutamique. Une autre cyclisation des polypeptides est fabriquée en formant des liaisons éther entre les chaînes latérales de la terminal C et de la sérine ou de la thréonine.
(3) Type de borne ou de tête à queue
Les polypeptides de la chaîne peuvent être cyclées dans un solvant ou fixés sur une résine par cyclation de la chaîne latérale. De faibles concentrations de peptides doivent être utilisées dans la centralisation des solvants pour éviter l'oligomérisation des peptides. Le rendement d'un polypeptide annulaire synthétique de la tête à la tête dépend de la séquence du polypeptide de la chaîne. Par conséquent, avant de préparer les peptides cycliques à grande échelle, une bibliothèque de peptides de plomb à chaînes possibles doit d'abord être créée, suivie d'une cyclisation pour trouver la séquence avec les meilleurs résultats.
2. N-méthylation
La N-méthylation se produit à l'origine dans les peptides naturels et est introduit dans la synthèse des peptides pour empêcher la formation de liaisons hydrogène, rendant ainsi les peptides plus résistants à la biodégradation et à la clairance. La synthèse des peptides utilisant des dérivés d'acides aminés N-méthylés est la méthode la plus importante. De plus, la réaction de Mitsunobu des intermédiaires de polypeptide-résine N- (2-nitrobenzène sulfonyle) peut également être utilisée. Cette méthode a été utilisée pour préparer des bibliothèques peptidiques cycliques contenant des acides aminés N-méthylés.
3. Phosphorylation
La phosphorylation est l'une des modifications post-traductionnelles les plus courantes dans la nature. Dans les cellules humaines, plus de 30% des protéines sont phosphorylées. La phosphorylation, en particulier la phosphorylation réversible, joue un rôle important dans le contrôle de nombreux processus cellulaires, tels que la transduction du signal, l'expression des gènes, le cycle cellulaire et la régulation du cytosquelette et l'apoptose.
La phosphorylation peut être observée dans une variété de résidus d'acides aminés, mais les cibles de phosphorylation les plus courantes sont les résidus de sérine, de thréonine et de tyrosine. Les dérivés de phosphotyrosine, de phosphothréonine et de phosphosérine peuvent être introduits dans les peptides pendant la synthèse ou formés après synthèse des peptides. La phosphorylation sélective peut être obtenue en utilisant des résidus de sérine, de thréonine et de tyrosine qui éliminent sélectivement les groupes de protection. Certains réactifs de phosphorylation peuvent également introduire des groupes d'acide phosphorique dans le polypeptide par post-modification. Ces dernières années, la phosphorylation spécifique au site de la lysine a été obtenue en utilisant une réaction de staudinger-phosphite chimiquement sélective (figure 3).

4. Myristoylation et palmitoylation
L'acylation du N-terminal avec les acides gras permet aux peptides ou aux protéines de se lier aux membranes cellulaires. La séquence myridamoylée sur le N-terminal N-terminal permet à la cible des protéines de la famille SRC et des protéines de transcriptase inverse de se lier aux membranes cellulaires. L'acide myristique était lié au N-terminal de la résine-polypeptide en utilisant des réactions de couplage standard, et le lipopeptide résultant pourrait être dissocié dans des conditions standard et purifié par RP-HPLC.
5. Glycosylation
Les glycopeptides tels que la vancomycine et la téicolanine sont des antibiotiques importants pour le traitement des infections bactériennes résistantes au médicament, et d'autres glycopeptides sont souvent utilisés pour stimuler le système immunitaire. De plus, comme de nombreux antigènes microbiens sont glycosylés, il est d'une grande importance d'étudier les glycopeptides pour améliorer l'effet thérapeutique de l'infection. D'un autre côté, il a été constaté que les protéines de la membrane cellulaire des cellules tumorales présentent une glycosylation anormale, ce qui fait que les glycopeptides jouent un rôle important dans la recherche sur le cancer et la défense immunitaire tumorale. Les glycopeptides sont préparés par la méthode FMOC / T-BU. Des résidus glycosylés, tels que la thréonine et la sérine, sont souvent introduits dans les polypeptides par des FMOC activés par l'ester de pentafluorophénol pour protéger les acides aminés glycosylés.
6. Isoprène
L'isopentadiénylation se produit sur les résidus de cystéine dans la chaîne latérale près du C-terminal. La protéine isoprène peut améliorer l'affinité de la membrane cellulaire et former l'interaction protéine-protéine. Les protéines isopentadiées comprennent la tyrosine phosphatase, la petite gtase, les molécules de cochaperone, la lame nucléaire et les protéines de liaison centromériques. Les polypeptides d'isoprène peuvent être préparés à l'aide d'isoprène sur des résines ou en introduisant des dérivés de cystéine.
7. Modification du polyéthylène glycol (PEG)
La modification du PEG peut être utilisée pour améliorer la stabilité hydrolytique des protéines, la biodistribution et la solubilité des peptides. L'introduction de chaînes PEG aux peptides peut améliorer leurs propriétés pharmacologiques et également inhiber l'hydrolyse des peptides par des enzymes protéolytiques. Les peptides PEG traversent plus facilement la section transversale capillaire glomérulaire que les peptides ordinaires, réduisant considérablement la clairance rénale. En raison de la demi-vie active étendue des peptides PEG in vivo, le niveau de traitement normal peut être maintenu avec des doses plus faibles et des peptides moins fréquents. Cependant, la modification du PEG a également des effets négatifs. De grandes quantités de PEG empêchent l'enzyme de dégrader le peptide et de réduire également la liaison du peptide au récepteur cible. Mais la faible affinité des peptides PEG est généralement compensée par leur demi-vie pharmacocinétique plus longue, et en étant présents dans le corps plus longtemps, les peptides PEG ont une plus grande probabilité d'être absorbé dans les tissus cibles. Par conséquent, les spécifications du polymère PEG doivent être optimisées pour des résultats optimaux. D'un autre côté, les peptides PEG s'accumulent dans le foie en raison d'une clairance rénale, entraînant un syndrome macromoléculaire. Par conséquent, les modifications de PEG doivent être conçues plus attentivement lorsque les peptides sont utilisés pour les tests de médicaments.

Les groupes de modification communs des modificateurs de PEG peuvent être à peu près résumés comme suit: amino (-amine) -NH2, aminométhyl-ch2-nh2, hydroxy-oh, carboxy-cooh, sulfhydryl (-thiol) -sh, malémide -mal, carbonate de succimide -sc, acétate de succine -scmique, succimide - spaate-espa, acétate -cétate -scmique, succimide - spaate, acétate de succine -scmique, succimide - spaate-espa, acétate -cétate -scmique, succimide - spaate-espa, acétate de succine -scmique, succilide - spaate-espa, succinimide -scmique, succimide Promesse n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (such as propional-ald, butyrALD), acrylic base (-acrylate-acrl), azido-azide, biotinyl -Biotin, Fluorescein, glutaryl -GA, Acrylate Hydrazide, alkyne-alkyne, P-toluenesulfonate -oTs, succinide succinate -SS, etc. Les dérivés PEG avec des acides carboxyliques peuvent être couplés à des amines N-terminales ou à des chaînes latérales de lysine. La PEG activée par l'amio peut être couplée à des chaînes latérales d'acide aspartique ou d'acide glutamique. Le PEG activé par mal-parole peut être conjugué à Mercaptan de chaînes latérales de cystéine entièrement déprotégées [11]. Les modificateurs de PEG sont généralement classés comme suit (Remarque: MPEG est méthoxy-PEG, CH3O- (CH2CH2O) N-CH2CH2-OH):
(1) Modificateur de cheville à chaîne droite
MPEG-SC, MPEG-SCM, MPEG-SPA, MPEG-OT, MPEG-SH, MPEG-ALD, MPEG-BUTYRALD, MPEG-SS
(2) modificateur de PEG bifonctionnel
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCL · NH2-PEG-COOH, MAL-PEG-NHS
(3) Modificateur de cheville de ramification
(MPEG) 2-NHS, (MPEG) 2-ALD, (MPEG) 2-NH2, (MPEG) 2-MAL
8. Biotinisation
La biotine peut être fortement liée à l'avidine ou à la streptavidine, et la résistance de liaison est même proche de la liaison covalente. Les peptides marqués par la biotine sont couramment utilisés dans l'immunoessai, l'histocytochimie et la cytométrie d'écoulement basée sur la fluorescence. Les anticorps antibiotine marqués peuvent également être utilisés pour se lier aux peptides biotinylés. Les étiquettes de biotine sont souvent attachées à la chaîne latérale de la lysine ou au terminal n. L'acide 6-aminocaproïque est souvent utilisé comme liaison entre les peptides et la biotine. La liaison est flexible dans la liaison au substrat et se lie mieux en présence d'un obstacle stérique.
9. Étiquetage fluorescent
Le marquage fluorescent peut être utilisé pour tracer les polypeptides dans les cellules vivantes et pour étudier les enzymes et les mécanismes d'action. Le tryptophane (TRP) est fluorescent, il peut donc être utilisé pour le marquage intrinsèque. Le spectre d'émission du tryptophane dépend de l'environnement périphérique et diminue avec la diminution de la polarité du solvant, une propriété utile pour détecter la structure des peptides et la liaison des récepteurs. La fluorescence du tryptophane peut être éteinte par l'acide aspartique protoné et l'acide glutamique, ce qui peut limiter son utilisation. Le groupe de chlorure de dans-pantyle (Dansyle) est très fluorescent lorsqu'il est lié à un groupe amino et est souvent utilisé comme étiquette fluorescente pour les acides aminés ou les protéines.
La conversion d'énergie de résonance de fluorescence (FRET) est utile pour les études enzymatiques. Lorsque la frette est appliquée, le polypeptide du substrat contient généralement un groupe de marquage de fluorescence et un groupe de déchargement de fluorescence. Les groupes fluorescents marqués sont éteintes par l'extincteur grâce à un transfert d'énergie non photonique. Lorsque le peptide est dissocié de l'enzyme en question, le groupe de marquage émet une fluorescence.
10. Cage Polypeptides
Les peptides de cage ont des groupes de protection optiquement amovibles qui protègent le peptide de la liaison au récepteur. Lorsqu'elle est exposée au rayonnement UV, le peptide est activé, restaurant son affinité avec le récepteur. Étant donné que cette activation optique peut être contrôlée en fonction du temps, de l'amplitude ou de l'emplacement, les peptides de cage peuvent être utilisés pour étudier les réactions survenant dans les cellules. Les groupes de protection les plus couramment utilisés pour les polypeptides de cage sont les groupes 2-nitrobenzyle et leurs dérivés, qui peuvent être introduits dans la synthèse des peptides via des dérivés protecteurs d'acides aminés. Les dérivés d'acides aminés qui ont été développés sont la lysine, la cystéine, la sérine et la tyrosine. Cependant, les dérivés de l'aspartate et du glutamate ne sont pas couramment utilisés en raison de leur sensibilité à la cyclisation pendant la synthèse et la dissociation des peptides.
11. peptide polyantigène (carte)
Les peptides courts ne sont généralement pas immunisés et doivent être couplés aux protéines porteurs pour produire des anticorps. Le peptide polyantigène (MAP) est composé de multiples peptides identiques connectés aux noyaux de lysine, qui peuvent exprimer spécifiquement les immunogènes de puissance élevée et peuvent être utilisés pour préparer des couplets protéiques de carrier peptidique. Les polypeptides MAP peuvent être synthétisés par synthèse de phase solide sur la résine MAP. Cependant, un couplage incomplet entraîne des chaînes peptidiques manquantes ou tronquées sur certaines branches et ne présente donc pas les propriétés du polypeptide de carte d'origine. Comme alternative, les peptides peuvent être préparés et purifiés séparément puis couplés à la carte. La séquence peptidique attachée au noyau du peptide est bien définie et facilement caractérisée par la spectrométrie de masse.
Conclusion
La modification des peptides est un moyen important de concevoir des peptides. Les peptides chimiquement modifiés peuvent non seulement maintenir une activité biologique élevée, mais également éviter efficacement les inconvénients de l'immunogénicité et de la toxicité. Dans le même temps, la modification chimique peut doter des peptides avec de nouvelles excellentes propriétés. Ces dernières années, la méthode d'activation C-H pour la post-modification des polypeptides a été rapidement développée et de nombreux résultats importants ont été obtenus.
Heure du poste: 2025-07-03
